Đề kiểm tra cuối học kì 2 Hóa học Lớp 8
I. Trắc nghiệm: (4đ) Khoanh tròn vào đáp án đúng:
Câu 1: Nguyên liệu nào sau đây được sử dụng để điều chế oxi trong PTN?
A. KMnO4 B. Fe2O3 C. Fe2O3 D. H2O
Câu 2: Người ta thu khí oxi bằng cách đẩy nước là nhờ dựa vào tính chất:
A. Khí oxi tan trong nước B. Khí oxi ít tan trong nước
C. Khí oxi khó hoá lỏng D. Khí oxi nhẹ hơn nước
Câu 3: Thành phần của không khí gồm:
A. 21% oxi, 1% nitơ, 78% các khí khác.
C. 78% nitơ, 21% oxi, 1% các khí khác B. 78% nitơ, 1% oxi, 21% các khí khác.
D. 78% oxi, 21% nitơ, 1% các khí khác
Câu 4: Quả bóng bay bơm khí hidro bay được là do
A. khí Hidro nặng hơn không khí. B. khí Hidro nhẹ hơn khí Oxi.
C. khí Hidro nhẹ hơn khí Oxi. D. khí Hidro nhẹ hơn không khí.
Bạn đang xem tài liệu "Đề kiểm tra cuối học kì 2 Hóa học Lớp 8", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
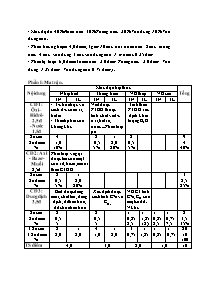
- Mức độ đề: 40% Nhận biết; 30% Thông hiểu; 20% Vận dụng; 10% Vận dụng cao. - Phần trắc nghiệm: 4,0 điểm, (gồm 16 câu hỏi: nhận biết: 8 câu, thông hiểu: 4 câu, vận dụng: 3 câu vận dụng cao: 1 mỗi câu 0,25điểm; - Phần tự luận: 6,0 điểm (nhận biết: 2,0 điểm Thông hiểu: 2,0 điểm; Vận dụng: 1,25 điểm; Vận dụng cao: 0,75 điểm). Phần I: Ma trận. Nội dung Mức độ nhận thức Tổng Nhận biết Thông hiểu VD thấp VD cao TN TL TN TL TN TL TN TL CĐ 1: Ôxi – Hiđrô- 2,5 đ -Nước 1,5đ - T/c hoá học và cách đ/c của oxi, hiđro - Thành phần của không khí. Viết được PTHH thuộc tính chất và đ/c oxi, hidro, nước ...Phân loại pư Tính theo PT HH xác định khối lượng H2O Số câu Số điểm % 4 1,0 10% 2 0,5 5% 1 2,0 20% 2 0,5 5% 9 4 40% CĐ 2: Axit - Bazơ- Muối 2,5đ Phân loại và gọi được tên của một số oxit, bazơ, muối theo CTHH Số câu Số điểm % 2 0,5 5% 1 2,0 20% 3 2,5 25% CĐ 3: Dung dịch 3,5đ Biết được dung môi, chất tan, dung dịch, dd bão hòa, dd chưa bão hòa Xác định được cách tính C% và CM. VD CT tính C%, CM của một số dd. V khí. Số câu Số điểm % 2 0,5 5 2 0,5 5 1 0,25 2,5 1 1,25 12,5 1 0,25 2,5 1 0,75 7,5 8 3,5 35% T Số câu T Số điểm % 8 2,0 1 2,0 4 1,0 1 2,0 3 0,75 1 1,25 1 0,25 1 0,75 20 10 100 TS điểm 4,0 3,0 2,0 1,0 10 Phần II: Đề bài. I. Trắc nghiệm: (4đ) Khoanh tròn vào đáp án đúng: Câu 1: Nguyên liệu nào sau đây được sử dụng để điều chế oxi trong PTN? A. KMnO4 B. Fe2O3 C. Fe2O3 D. H2O Câu 2: Người ta thu khí oxi bằng cách đẩy nước là nhờ dựa vào tính chất: A. Khí oxi tan trong nước B. Khí oxi ít tan trong nước C. Khí oxi khó hoá lỏng D. Khí oxi nhẹ hơn nước Câu 3: Thành phần của không khí gồm: A. 21% oxi, 1% nitơ, 78% các khí khác. C. 78% nitơ, 21% oxi, 1% các khí khác B. 78% nitơ, 1% oxi, 21% các khí khác. D. 78% oxi, 21% nitơ, 1% các khí khác Câu 4: Quả bóng bay bơm khí hidro bay được là do A. khí Hidro nặng hơn không khí. B. khí Hidro nhẹ hơn khí Oxi. C. khí Hidro nhẹ hơn khí Oxi. D. khí Hidro nhẹ hơn không khí. Câu 5: Sản phẩm của phản ứng giữa hiđro và Chì(II)oxit là gì? A. chì và nước. C. đồng và oxi. B. oxi và nước. D. hiđro và oxi. Câu 6: Thu khí hidro bằng các đẩy không khí ta đặt bình như thế nào? A. Úp bình B. Ngửa bình C. Nghiêng bình D. Không thu được Câu 7: Phản ứng nào sau đây thuộc loại phản ứng phân hủy: A. 2KClO3 t 2KCl + 3O2 B. Fe2O3 + H2 Fe + H2O C. 2H2O ĐF H2 + O2 D. FeCl2 + Cl2 t FeCl3 Câu 8: Đốt 20ml khí H2 trong 20 ml khí O2. Sau khi đưa về nhiệt độ và áp suất ban đầu, thể tích còn dư sau phản ứng là? A. Dư 10ml O2 B. Dư 10ml H2 C. hai khí vừa hết D. Không xác định được Câu 9: Dãy chất nào chỉ toàn bao gồm axit: A. HCl; NaOH B. CaO; H2SO4 C. H3PO4; HNO3 D. SO2; KOH Câu 10: Dãy chất nào chỉ toàn bao gồm muối: A. MgCl; Na2SO4; KNO3 B. Na2CO3; H2SO4; Ba(OH)2 C. CaSO4; HCl; MgCO3 D. H2O; Na3PO4; KOH Câu 11: Các câu sau, câu nào đúng khi định nghĩa dung dịch? A. Dung dịch là hỗn hợp đồng nhất của chất rắn và chất lỏng B. Dung dịch là hỗn hợp đồng nhất của chất khí và chất lỏng C. Dung dịch là hỗn hợp đồng nhất của hai chất lỏng D. Dung dịch là hỗn hợp đồng nhất của chất tan và dung môi Câu 12: Độ tan của một chất trong nước ở một nhiệt độ xác định là: A. Số gam chất đó có thể tan trong 100g dung dịch B. Số gam chất đó có thể tan trong 100g nước C. Số gam chất đó có thể tan trong 100g dung môi để tạo thành dung dịch bão hoà D. Số gam chất đó có thể tan trong 100g nước để tạo thành dung dịch bão hoà Câu 13: Để tính nồng độ mol của dung dịch NaOH, người ta làm thế nào? A. Tính số gam NaOH có trong 100g dung dịch B. Tính số gam NaOH có trong 1 lít dung dịch C. Tính số gam NaOH có trong 1000g dung dịch D. Tính số mol NaOH có trong 1 lít dung dịch Câu 14: Để tính nồng độ phần trăm của dung dịch HCl, người ta làm thế nào? A. Tính số gam HCl có trong 100g dung dịch B. Tính số gam HCl có trong 1lít dung dịch C. Tính số mol HCl có trong 100g dung dịch D. Tính số mol HCl có trong 1lít dung dịch Câu 15: Hòa tan 5g đường vào 45g nước dung dịch thu được có nồng độ phần trăm là: A. 7,5% B. 10% C. 12,5% D. 15% Câu 16: Độ tan của muối NaCl ở 1000C là 40g. ở nhiệt độ này dung dịch bão hoà NaCl có nồng độ phần trăm là: A. 28% B. 26,72% C. 28,57% D. 30,05% II. Tự luận: (6đ) Câu 17 (2 điểm): Hãy phân loại và gọi tên các hợp chất có công thức hoá học sau: HBr; ZnSO4; SO3; Fe(OH)2; Cu(OH)2; HNO3; Pb(NO3)2; Fe2O3. Câu 18 (2đ). Hãy hoàn thành các phương trình hóa học sau, cho biết các phản ứng đó thuộc loại phản ứng nào? Vì sao? a . P + O2 ? b . Fe + ? FeCl2 + H2 c . Al + ? Al2O3 d . ? Hg + O2 Câu 19 (2 điểm): Cho 500ml dung dịch HCl phản ứng vừa đủ với 6,5g Zn . a. Tính CM của dung dịch HCl đã phản ứng. b. Tính thể tích khí H2 tạo thành sau phản ứng. Biết khi thu khí Hidro bị hao hụt đi ¼ lần. Phần III: Đáp án. I. Trắc nghiệm (3đ): Mỗi câu đúng được 0,5đ Câu 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 ĐA A B C D A A C A C A D D D A B C II. Tự luận (7đ): Đề 1: Câu Đáp án Điểm 7 a. 4P + 5O2 2P2O5 Pư hóa hợp b. Fe + 2HCl FeCl2 + H2 Pư thế c. 4Al + 3O2 2Al2O3 Pư hoá hợp d. 2HgO 2Hg + O2 Pư phân hủy PƯ hóa hợp: a,c PƯ thế: b PƯ phân hủy: d Mỗi PT đúng 0,25đ. Phân loại đúng 1,0đ 8 Oxit: - SO3: Lưu huỳnh tri oxit. - Fe2O3: Sắt (III) oxit Axit: - HBr: Axit bromhiđric - HNO3: Axit nitric Bazơ: - Cu(OH)2: Đồng(II) hiđroxit - Fe(OH)2: Sắt(II) hiđroxit Muối: - ZnSO4: Kẽm sunfat - Pb(NO3)2: Chì (II) nitrat 0,5đ 0,5đ 0,5đ 0,5đ 9 - Số mol của kẽm : nZn = 6,5 / 65 = 0,1 (mol) PTHH : Zn + 2HCl ZnCl2 + H2 Theo PT : nHCl = 2. nZn = 2. 0,1 = 0,2( mol) Đổi 500ml = 0,5 l a) CM = CM( dd HCl) = 0,2 / 0,5 = 0,4(M) b) theo pt: nH2= nZn = 0, 1( mol) VH = 0,1 . 22,4 = 2,24 (l) vì khi thu khí bị hao hụt ¼ nên thể tích khí thu được là 2,24 .3/4 = 1,68 l 0,25đ 0,25đ 0,25đ 0,25đ 0,25đ 0,25đ 0,25đ 0,25 đ
Tài liệu đính kèm:
 de_kiem_tra_cuoi_hoc_ki_2_hoa_hoc_lop_8.docx
de_kiem_tra_cuoi_hoc_ki_2_hoa_hoc_lop_8.docx





