Ma trận đề kiểm tra học kì môn Hóa học 9
A . TRẮC NGHIỆM KHÁCH QUAN( 3Đ)
Chọn và khoanh tròn vào chữ cái đứng trước phương án trả lời đúng nhất
Câu 1: Phương pháp dùng để điều chế được sắt (III) hiđroxit là
a. Cho kim lọai sắt tác dụng với dung dịch natri hiđroxit
b. Cho muối sắt (II ) clorua tác dụng với đồng (II) hiđroxit
c. Cho muối sắt (III) sunfat tác dụng với dung dịch kali hiđroxit
d. Cho oxit sắt (III) tác dụng với dung dịch natri hiđroxit
Câu 2: Các chất đều tác dụng được với dung dịch HCl là
a. ZnO, CuO, CaO, SO2 b. CuO, CaO, ZnO, CO2
c. ZnO, CuO, CaO, P2O5 d. KOH, ZnO, CuO, CaO
Bạn đang xem tài liệu "Ma trận đề kiểm tra học kì môn Hóa học 9", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
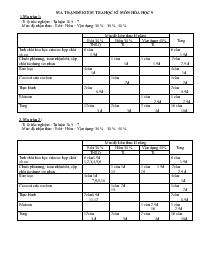
MA TRẬN ĐỀ KIỂM TRA HỌC KÌ MÔN HÓA HỌC 9 1.Ma trận 1: -Tỉ lệ trắc nghiệm : Tự luận là 3 : 7 -Mức độ nhận thức : Biết – Hiểu – Vận dụng: 30 % - 30 % - 40 % Mức độ kiến thức kĩ năng Tổng Biết 30 % Hiểu 30 % Vận dụng 40% TNKQ TL TL Tính chất hóa học của các hợp chất vô cơ 6 câu 1.5đ 6 câu 1.5đ Chuỗi phản ứng, toán nhận biết, cặp chất tác dụng với nhau 1 câu 1đ 1 câu 1.5đ 2câu 2.5 đ Kim loại 4câu 1đ 4câu 1đ Cac oxit của cacbon 1câu 2đ 1câu 2đ Thực hành 2câu 0.5đ 2câu 0.5đ Bài toán 1 câu 2.5đ 1 câu 2.5đ Tổng 12câu 3 đ 2câu 3đ 2 câu 4đ 16 câu 10đ 2. Ma trận 2 : -Tỉ lệ trắc nghiệm : Tự luận là 3 : 7 -Mức độ nhận thức : Biết – Hiểu – Vận dụng: 30 % - 30 % - 40 % Mức độ kiến thức kĩ năng Tổng Biết 30 % Hiểu 30 % Vận dụng 40% TNKQ TL TL Tính chất hóa học của các hợp chất vô cơ 6 câu 1.5đ 1,2,3,4,5,6 6 câu 1.5đ Chuỗi phản ứng, toán nhận biết, cặp chất tác dụng với nhau 1 câu 1đ 14 1 câu 1.5đ 15 2câu 2.5 đ Kim loại 4câu 1đ 7,8,9,10 4câu 1đ Cac oxit của cacbon 1câu 2đ 13 1câu 2đ Thực hành 2câu 0.5đ 11,12 2câu 0.5đ Bài toán 1 câu 2.5đ 16 1 câu 2.5đ Tổng 12câu 3 đ 2câu 3đ 2 câu 4đ 16 câu 10đ Sở GD & ĐT Lâm Đồng ĐỀ THI HỌC KÌ I NĂM HỌC 2009- 2010 Trường THCS- THPT Dân tộc nội trú MÔN THI: HÓA HỌC LỚP 9 ĐỀ 2: Thời gian : 45 phút (không kể thời gian phát đề) HỌ TÊN HS: . . . . . . . . . . . . . . . .. . . LỚP 9A . . . ĐIỂM: LỜI PHÊ CỦA CÔ GIÁO A . TRẮC NGHIỆM KHÁCH QUAN( 3Đ) Chọn và khoanh tròn vào chữ cái đứng trước phương án trả lời đúng nhất Câu 1: Phương pháp dùng để điều chế được sắt (III) hiđroxit là a. Cho kim lọai sắt tác dụng với dung dịch natri hiđroxit b. Cho muối sắt (II ) clorua tác dụng với đồng (II) hiđroxit c. Cho muối sắt (III) sunfat tác dụng với dung dịch kali hiđroxit d. Cho oxit sắt (III) tác dụng với dung dịch natri hiđroxit Câu 2: Các chất đều tác dụng được với dung dịch HCl là a. ZnO, CuO, CaO, SO2 b. CuO, CaO, ZnO, CO2 c. ZnO, CuO, CaO, P2O5 d. KOH, ZnO, CuO, CaO Câu 3: Để nhận biết axit sunfuric ta dùng chất nào trong các chất sau đây? a. CaCl2 b. BaCl2 c. NaCl d. FeCl2 Câu 4: Chất nào sau đây còn có tên gọi là “xút ăn da ”? a. Ca(OH)2 b. Cu(OH)2 c. Zn(OH)2 d. NaOH Câu 5: Phản ứng hóa học xảy ra khi cho muối tác dụng với axit, bazơ, muối gọi là a. Phản ứng phân huỷ b. Phản ứng trao đổi c. Phản ứng thế d. Phản ứng trung hòa Câu 6:Cặp chất tác dụng được với nhau là a. Na2CO3 + KCl b. NaCl + AgNO3 c. ZnSO4 + CuCl2 d. Na2SO4 +AlCl3 Câu 7: Dãy các kim loại được xếp theo chiều hoạt động hoá học tăng dần là a. K, Mg, Cu, Al, Zn, Fe b. Fe, Cu, K, Mg, Al, Zn c. Zn, K, Mg, Cu, Al, Fe d. Cu, Fe, Zn, Al, Mg, K Câu 8: Kim loại phản ứng được với axit sunfuric tạo ra muối và giải phóng hiđro là a. Nhôm, sắt b. Bạc, kẽm c. Đồng , chì d. Sắt, đồng Câu 9: Dụng cụ bằng kim loại nào không nên dùng để đựng nước vôi? a. Fe b. Ag c. Cu d. Al Câu 10: Cho các kim loại sau: Cu, Na, Al, Ba. Kim loại tác dụng được với axit tạo ra khí bay lên là a. Cu b. Ba c. Al d. Na Câu 11: Cho từ từ dung dịch NaOH vào dung dịch CuSO4, hiện tượng xảy ra là a. Có chất khí sinh ra b. Kết tủa bị tan ra c. Xuất hiện kết tủa trắng d. Xuất hiện kết tủa xanh lam Câu 12: Có các khí ẩm sau: CO2, SO2, O2. Hóa chất có thể dùng để làm khô chúng là a. H2SO4 b. CaO c. K2O d. Ca (OH)2 B.TỰ LUẬN(7Đ) Câu 13:Tìm điểm khác nhau về tính chất hoá học của CO và CO2.Viết phương trình hoá học (nếu có) (2đ) Câu 14: Viết các phương trình hóa học khi cho các cặp chất sau tác dụng với nhau (1đ) a. Sắt với lưu huỳnh b. Kali hiđroxit và axit clohiđric Câu 15: Viết phương trình hoá học ( kèm điều kiện) biểu diễn sơ đồ biến hoá sau ( 1.5đ) Fe FeCl3 Fe(OH)3 Fe2 (SO4)3 Câu 16: Hoà tan hoàn toàn 10g hỗn hợp gồm Al và Al2O3 vào dung dịch axit clohiđric dư thu được 6.72 lít khí hiđro (ở đktc).Tính thành phần phần trăm khối lượng các chất có trong hỗn hợp. (2.5đ) (Al=27 , O=16) ĐÁP ÁN HÓA 9 ĐỀ II A . TRẮC NGHIỆM KHÁCH QUAN( 3Đ) Chọn và khoanh tròn vào chữ cái có phương án trả lời đúng nhất. Mỗi câu trả lời đúng 0.25 đ 1 2 3 4 5 6 7 8 9 10 11 12 c d b d b b d a d c d a B.TỰ LUẬN(7Đ) Câu 13: CO CO2 Chaùy ñöôïc CO + O2 CO2 (0.25đñ) Coù tính khöû CO + FeO Fe + CO2 (0.25đñ) Khoâng phaûi laø oxit axit (0.25đñ) Khoâng chaùy ñöôïc (0.25đñ) Khoâng coù tính khöû (0.25đñ) Laø moät oxit axit :CO2 + H2O H2CO3 (0.25đñ) CO2 + Ca(OH)2 CaCO3 + H2O (0.25đñ) CO2 + CaO CaCO3 (0.25đñ) Câu 14: Fe + S FeS (0.5đñ) KOH + HCl KCl + H2O (0.5đñ) Câu 15: 2Fe + 3Cl2 2FeCl3 (0.5đñ) FeCl3 + 3 NaOH Fe(OH)3 ↓ + 3NaCl (0.5đñ) Fe(OH)3 + H2SO4 Fe2( SO4)3 + H2O (0.5đñ) Câu 16: n H2 = V : 22.4 = 6.72 : 22.4 = 0.3 mol (0.25đñ) - PTHH : 2 Al + 6 HCl 2AlCl3 + 3 H2 ↑ (0.5đñ) 2mol 6mol 2mol 3mol 0.2mol 0.3mol 2Al2O3 + 6 HCl 2AlCl3 + 3 H2O (0.5đñ) - Số gam Al đã dùng : - Theo PT : n Al = 0.2 mol -> m Al = n xM = 0.2 x 27 = 5.4 g (0.5đñ) m Al2O3 = 10 – 5.4 = 4.6 g (0.25đñ) - Thành phần phần trăm khối lượng : % Al = (5.4 x 100) / 10 = 54 % (0.25đñ) % Al2O3 = 100 – 54 = 46 % (0.25đñ) Sở GD & ĐT Lâm Đồng ĐỀ THI HỌC KÌ I NĂM HỌC 2009- 2010 Trường THCS- THPT Dân tộc nội trú MÔN THI: HÓA HỌC LỚP 9 ĐỀ 1 Thời gian : 45 phút (không kể thời gian phát đề) HỌ TÊN HS: . . . . . . . . . . . . . . . .. . . LỚP 9A . . . ĐIỂM: LỜI PHÊ CỦA CÔ GIÁO A . TRẮC NGHIỆM KHÁCH QUAN( 3Đ) Chọn và khoanh tròn vào chữ cái đúng trước phương án trả lời đúng nhất Câu 1: Canxi oxit (vôi sống) để lâu ngày trong không khí bị giảm chất lượng, nguyên nhân là do : a. Canxi oxit bị nhiệt phân hủy b. Canxi oxit tác dụng với khí cacbonic trong không khí tạo thành đá vôi c. Canxi oxit tác dụng với khí oxi trong không khí tạo thành đá vôi d. Canxi oxit tác dụng với khí nitơ trong không khí tạo thành đá vôi Câu 2: Các chất đều tác dụng được với dung dịch NaOH là : a. SO2, CO2, P2O5, CuO c. SO2, CO2, P2O5, SO3 b. SO2, CO2, P2O5, H2O d. KOH, SO2, CO2, P2O5 Câu 3: Dùng .. để nhận biết dung dịch axit clohiđric a. Nước b. Phenolphtalein c. Quỳ tím d. Kim loại mạnh Câu 4: Chất nào sau đây còn có tên gọi là “nước vôi trong ”? a. Ca(OH)2 b. Cu(OH)2 c. Zn(OH)2 d. NaOH Câu 5: Phản ứng hóa học xảy ra giữa axit với bazơ tạo thành muối và nước được gọi là a. Phản ứng hóa hợp b. Phản ứng thế c. Phản ứng trung hòa d. Phản ứng phân hủy Câu 6:Cho các chất sau: KOH, Mg(OH)2, CO2, HCl. Có bao nhiêu cặp chất tác dụng được với nhau? a. 3 cặp b. 4 cặp c. 5 cặp d. 6 cặp Câu 7: Dãy các kim loại được xếp theo chiều hoạt động hoá học giảm dần là a. K, Mg, Cu, Al, Zn, Fe . b. Fe, Cu, K, Mg, Al, Zn . c. Zn, K, Mg, Cu, Al, Fe . d. K, Mg, Al, Zn, Fe, Cu Câu 8: Dụng cụ bằng kim loại nào không nên dùng để đựng nước vôi? a. Fe b. Ag c. Cu d. Al Câu 9: Kim loại không tác dụng với axit sunfuric đặc, nguội là: a. Nhôm, kẽm b. Đồng, nhôm c. Đồng, sắt d. Nhôm, sắt Câu 10: Cho các kim loại sau: Cu, Na, Al, Ba. Kim loại tác dụng được với nước tạo ra khí bay lên là a. Cu, Na b. Al, Ba c. Na, Ba d. Na, Al Câu 11: Cho từ từ dung dịch NaOH vào ống nghiệm có chứa bột nhôm và sắt, hiện tượng xảy ra là a. Một ống có bọt khí thoát ra b. Hai ống có bọt khí thoát ra c. Một ống có kết tủa trắng d. Một ống tạo bọt khí, một ống tạokết tủa Câu 12: Sau khi làm thí nghiệm, có những khí đôc hại thải ra là: HCl, H2S, CO2, SO2. Chất được dùng để loại bỏ chúng tốt nhất là a. Nước vôi trong b. Dung dịch HCl c. Dung dịch NaCl d. Nước B.TỰ LUẬN(7Đ) Câu 13: Viết các phương trình hóa học chứng minh cacbon oxit có tính khử, cacbon đioxit là một oxit axit? (2 đ) Câu 14: Viết các phương trình hóa học khi cho các cặp chất sau tác dụng với nhau. (1đ) a. Natri hiđroxit và kẽm clorua b. Nhôm với lưu huỳnh Câu 15: Có 3 lọ hóa chất mất nhãn chứa các dung dịch NaOH, BaCl2, AgCl. Em hãy nêu phương pháp hoá học để nhận biết ra từng chất. (1.5đ) Câu 16: Cho 21.6g hỗn hợp bột sắt và sắt (III) oxit vào dung dịch axit clohiđric dư thu được 2.24 lít khí hiđro (ở đktc) a.Tính khối lượng bột sắt và sắt (III) oxit chứa trong hỗn hợp đó. b. Tính khối lượng mỗi muối tạo thành. (2.5đ) ( Fe = 56, O = 16, H= 1, Cl = 35.5) ĐÁP ÁN HÓA 9 ĐỀ I A . TRẮC NGHIỆM KHÁCH QUAN( 3Đ) Chọn và khoanh tròn vào chữ cái có phương án trả lời đúng nhất. Mỗi câu trả lời đúng 0.25 đ 1 2 3 4 5 6 7 8 9 10 11 12 b c c a c b d d d c a a B.TỰ LUẬN(7Đ) Câu 13: Đối với CO : CO + FeO Fe + CO2 (0.5đ) Đối với CO2: CO2 + H2O H2CO3 (0.5đ) CO2 + Ca(OH)2 CaCO3 + H2O(0.5đ) CO2 + CaO CaCO3 (0.5đ) (HS có thể viết các PTHH khác ) Câu 14: 2NaOH + ZnCl2 Zn(OH)2 ↓ + 2NaCl (0.5đ) Al + S Al2S3 (0.5đ) Câu 15: - Thực hiện từng lượng nhỏ hoá chất (0,25đ) - Cho quỳ tím vào 3 dung dịch trên, chất nào làm quỳ tím hoá xanh là NaOH (0,25đ) - Cho H2SO4 vào 2 dung dịch còn lại dung dịch nào xuất hiện kết tủa trắng là BaCl2 (0,25đ) Phương trình H2SO4 + BaCl2 BaSO4 ↓+ 2HCl (0,5đ) - Chất còn lại là CuCl2 (0,25đ) Câu 16: nH2 = 0.1 mol ( 0.25đ) a. Phương trình hóa học: Fe + 2HCl FeCl2 + H2 ↑ (1) (0.5đ) 1mol 1mol 1mol 0.1mol 0.1mol 0.1mol Fe2O3 + 6HCl 2 FeCl3 + H2O (2) (0.25đ) 1mol 2mol 1mol 0.1mol 0.2mol Theo (1) thì nFe = 0.1mol (0.25đ) mFe = 5.6g (0.25đ) m Fe2O3 = 21.6 – 5.6=16 g (0.25đ) b. n FeCl2 = 0.1mol m FeCl2 = 0.1 x 127 = 12.7 g (0.25đ) n Fe2O3 = 16/160 = 0.1 mol (0.25đ) n FeCl3 = 0.2mol m FeCl3 = 0.2 x 162.5 = 32.5 g (0.25đ) Câu 2: (1,5đ)
Tài liệu đính kèm:
 de kiem tra.doc
de kiem tra.doc





